الإلكترونات الذرية
طاقة الإلكترون الذري
طاقة الإلكترون الذري مقدار سالب من الطاقة، ويكافئ المقدار الأدنى من الطاقة الذي يجب منحه للإلكترون لكي يتمكن من مغادرة الذرة.
التوابع الموجية للإلكترونات الذرية
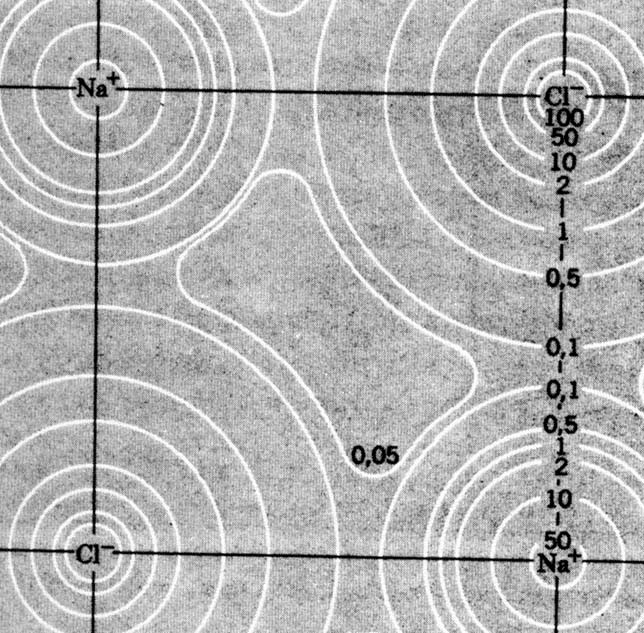
تصف فيزياء الكم quantum physics الإلكترونات الذرية بتابع موجي wave function يحدد احتمال probability وجود الإلكترون في مكان معين في لحظة معينة، ومن هنا يأتي مفهوم السحابة الإلكترونية electronic cloud المحيطة بالنواة، والتي تمثل التابع الاحتمالي لتوزع الكثافة الإلكترونية electron density. يمكن قياس توزع الكثافة الإلكترونية مثلاً بطريقة انعراج الأشعة السينية X-ray diffraction. يظهر الشكل التالي توزع الكثافة الإلكترونية في مقطع للبلورة NaCl ، والذي تم قياسه بطريقة انعراج الأشعة السينية.
-

توزع الكثافة الإلكترونية في مقطع للبلورة NaCl تم قياسه بطريقة انعراج الأشعة السينية. الخطوط المتصلة هي خطوط قيمة ثابتة للكثافة الإلكترونية.
يتم تصنيف التوابع الموجية للإلكترونات الذرية باستخدام أربعة أعداد كمومية quantum numbers:
1- العدد الطبقي shell number ![]() :
:
يأخذ هذا العدد القيم:
...![]()
ويسمى بالطبقي لتقارب طاقات الإلكترونات التي لها نفس العدد الطبقي، بحيث تعتبر طبقة طاقية واحدة، وتسمى هذه الطبقات بالطبقة ![]()
![]() وهي الطبقة ذات الطاقة الأدنى، تليها الطبقة
وهي الطبقة ذات الطاقة الأدنى، تليها الطبقة ![]()
![]() ، فالطبقة
، فالطبقة ![]()
![]() ، وهكذا.
، وهكذا.
2- عدد الاندفاع الزاوي momentum number ![]() :
:
ويمثل الاندفاع الزاوي للتابع الموجي للإلكترون، ويأخذ القيم الصحيحة التالية:
![]()
بحيث تقسم الطبقة الواحدة إلى طبقات جزئية sub-shells وفقاً لقيم هذا العدد، وتسمى الطبقات الجزئية l=0) s ، (l=1) p ، (l=2) d ، (l=3) f)، وهكذا.
3- عدد مركبة component الاندفاع الزاوي في اتجاه فراغي معين أو العدد المغناطيسي ![]() :
:
يدعى الاتجاه الفراغي المختار بالقطبي polar، ويأخذ هذا العدد القيم الصحيحة التالية:
![]()
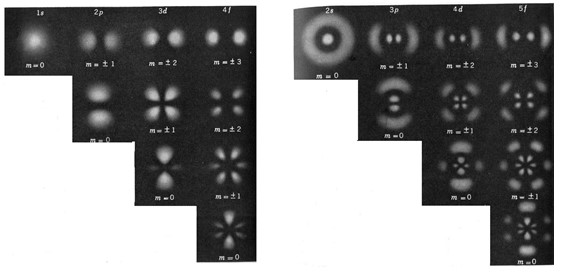
تحدد الأعداد الثلاثة ![]() التوزع الفراغي space distribution للكثافة الاحتمالية للإلكترون، ويظهر الشكل التالي هذا التوزع.
التوزع الفراغي space distribution للكثافة الاحتمالية للإلكترون، ويظهر الشكل التالي هذا التوزع.
4- السبين ![]() (s):
(s):
ويمثل الاندفاع الزاوي الذاتي eigenmomentum للإلكترون، ويأخذ إحدى القيمتين ± ½ ، ولهذا العدد الكمي مدلول إحصائي، فالقيمة الكسرية لسبين الإلكترون تعني أنه لا يجوز أن يكون لإلكترونين في الذرة الواحدة الأعداد الكمومية الأربعة نفسها، وهذا يضع حداً لعدد الإلكترونات التي تستطيع كل طبقة أو طبقة جزئية احتوائها.
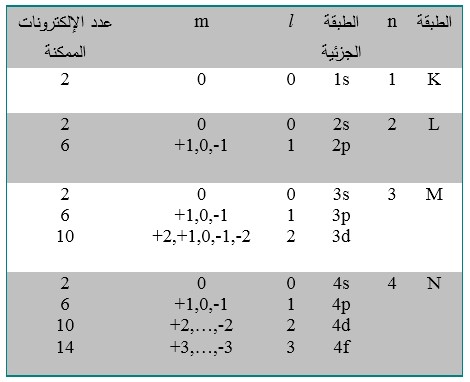
يوضح الجدول البنية الطبقية shell structure للإلكترونات الذرية مع عدد الإلكترونات الممكن تواجدها في كل طبقة جزئية.
نموذج بور الذري
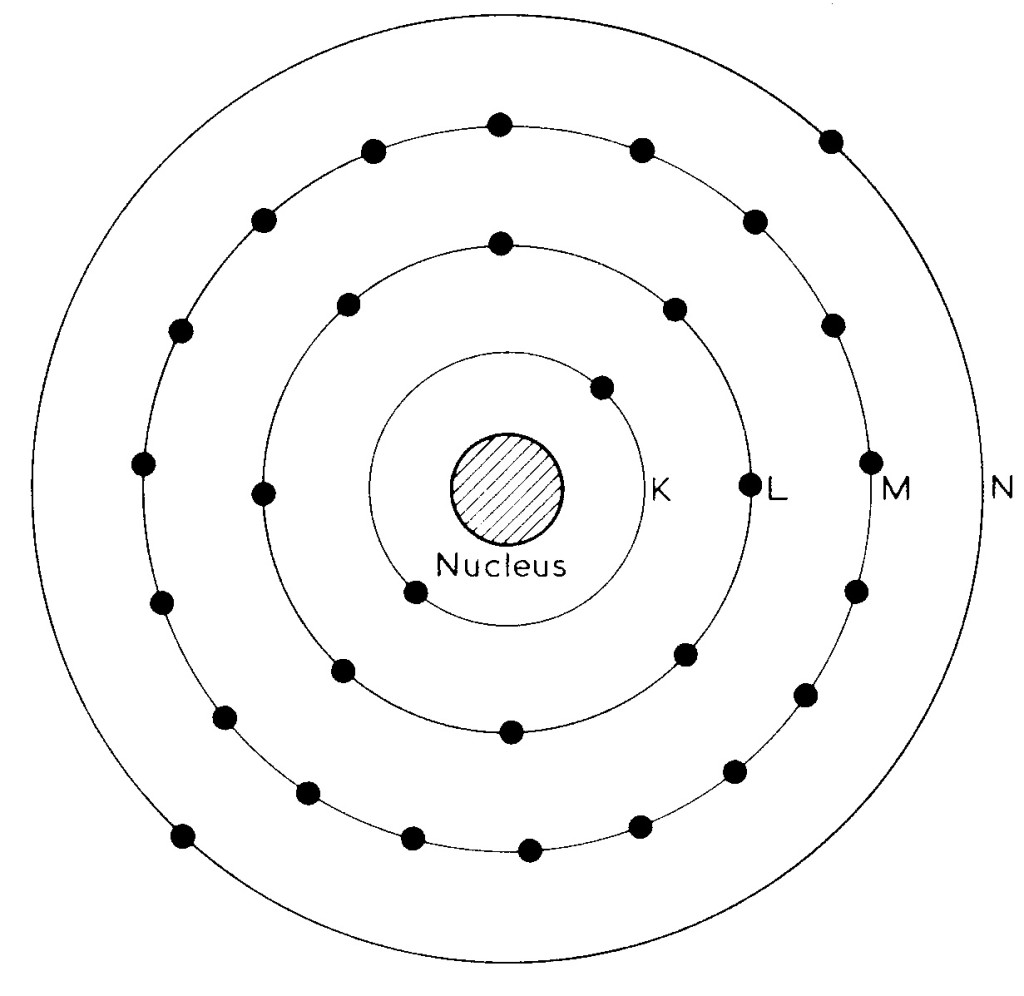
في نموذج بور Bohr model الذري يتم تمثيل الطبقات الطاقية بمدارات orbits حول النواة، ويساعد هذا النموذج في تبسيط فهم بعض الظواهر المرتبطة بالإلكترونات الذرية. يوضح الشكل التالي نموذج بور الذري ويظهر الطبقات الإلكترونية للزنك (Zn)، وهو عنصر يضم 30 إلكتروناً.
الحالة الدنيا للذرة، تهييج الذرة، وتأين الذرة
الحالة الدنيا ground state للذرة هي الحالة التي تتواجد فيها الإلكترونات الذرية في السويات الطاقية energy levels المتاحة اعتباراً من السوية الطاقية الأدنى فالتي تليها من حيث الطاقة وهكذا. ويمكن تهييج excitation الذرة بنقل أحد الإلكترونات أو أكثر من سويته الطاقية التي يتواجد فيها في الحالة الدنيا إلى سوية طاقية أعلى، في حال توفر شاغر في هذه السوية الأعلى، وذلك بمنحه مقداراً من الطاقة يعادل الفرق في الطاقة بين السويتين، وتسعى الذرة المهيجة إلى العودة إلى الحالة الدنيا بإعادة تنظيم الإلكترونات، وطرح الطاقة الفائضة على شكل كم Quanta أو كمات من الطاقة، فوتونات Photons، تحمل الفرق في الطاقة بين السوية الأعلى والسوية الأدنى. نظراً لاختلاف السويات الطاقية من عنصر لآخر، فإن هذه الفوتونات تميز العنصر الذي صدرت عنه.
أما إذا كانت طاقة التهيج تفوق طاقة الإلكترون الذري، فإنها تسمح للإلكترون بمغادرة الذرة، وبالتالي تتحول الذرة إلى أيون ion يحمل شحنة إجمالية موجبة.
المصدر: محاضرات د. سامي حداد في الفيزياء النووية – جامعة دمشق
تحرير: سامر عبد الرزاق بكر